合作研究人员发现,疟疾寄生虫通过一种称为转移核糖核酸(tRNA)修饰的细胞过程对抗疟药物(特别是青蒿素(ART))产生耐药性。 tRNA 修饰是一种机制,允许细胞通过改变细胞内的 RNA 分子来快速响应压力。

这一发现增进了对疟疾寄生虫如何应对药物引起的应激并产生耐药性的理解,并为开发抗击耐药性的新药铺平了道路。
疟疾是一种由蚊子传播的疾病,2022 年全球有 2.49 亿人遭受疟疾困扰,并造成 608,000 人亡。基于 ART 的联合疗法将 ART 衍生物与伙伴药物相结合,是无并发症疟疾患者的一线治疗方法。
ART 化合物有助于减少治疗前三天的寄生虫数量,而配合药物则可以消除剩余的寄生虫。然而,恶性疟原虫(P. falciparum)是导致人类疟疾的最致命的疟原虫物种,它正在对抗逆转录病治疗产生部分耐药性。这种部分耐药性在东南亚广泛存在,现已在非洲发现。
在一篇题为“ tRNA修饰重编程有助于恶性疟原虫对青蒿素耐药性”的论文中,新加坡麻省理工学院研究与技术联盟(SMART)抗生素耐药性跨学科研究小组的研究人员在《自然微生物学》上发表了一篇论文,该联盟是麻省理工学院在新加坡的研究企业。与麻省理工学院 (MIT)、哥伦比亚大学欧文医学中心和新加坡南洋理工大学合作,记录了这一新发现——单个 tRNA 的变化,tRNA 是一种小 RNA 分子,参与将遗传信息从 RNA 翻译成蛋白质,为疟疾寄生虫提供克服药物应激的能力。
该研究描述了 tRNA 修饰如何改变寄生虫对 ART 的反应,并通过改变其蛋白质表达谱来帮助其生存 ART 诱导的应激,使寄生虫对药物更具抵抗力。 ART 部分耐药性会导致基于 ART 的联合疗法治疗后疟疾寄生虫根除的延迟,从而使这些疗法效果较差,并且容易导致治疗失败。
“疟疾对目前最后一线抗疟药物青蒿素的耐药性日益增强,这是一场全球危机,需要新的策略和治疗方法。这种耐药性背后的机制复杂且多方面,但我们的研究揭示了一个关键联系。我们发现,疟原虫的致命剂量青蒿素的存活能力与特定 tRNA 修饰的下调有关,这一发现为应对这一日益严重的全球威胁的新策略铺平了道路,”该部门医学助理教授 Jennifer L. Small-Saunders 说。 CUIMC 传染病学博士,该论文的第一作者。
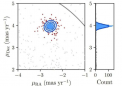
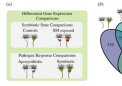
研究人员利用 SMART 开发的先进表观转录组分析技术,研究了表观转录组学(细胞内 RNA 修饰的研究)在影响疟疾耐药性方面的作用。这涉及分离感兴趣的 RNA、tRNA,并使用质谱法来识别存在的不同修饰。
他们分离并比较了药物敏感和耐药的疟原虫,其中一些接受了抗逆转录病治疗,另一些则作为对照未经治疗。分析揭示了耐药寄生虫的 tRNA 修饰发生了变化,这些修饰与寄生虫中特定基因翻译的增加或减少有关。
人们发现翻译过程的改变是观察到的耐药性增加的潜在机制。这一发现还拓展了我们对微生物和癌细胞如何利用 RNA 修饰的正常功能来阻止药物和其他疗法的性作用的理解。
“我们的研究是同类研究中的首例,展示了 tRNA 修饰如何直接影响寄生虫对 ART 的抵抗力,强调了 RNA 修饰对疾病和健康的潜在影响。虽然 RNA 修饰已经存在了几十年,但它们在调节细胞过程中的作用SMART AMR 联合首席研究员、麻省理工学院教授、研究人员之一 Peter Dedon 表示:“我们的研究结果强调了 RNA 修饰对研究界的重要性,以及 tRNA 修饰在调节基因表达方面的更广泛意义。”该论文的作者。
“在 SMART AMR,我们处于探索传染病和抗菌素耐药性表观转录组学的前沿。表观转录组学是疟疾研究的一个新兴领域,在疟疾寄生虫的发育和应激反应中发挥着至关重要的作用,”Co. Peter Preiser 说-SMART AMR 首席研究员、新加坡南洋理工大学分子遗传学和细胞生物学教授,也是该论文的作者之一。
“这一发现揭示了耐药寄生虫如何利用表观转录组应激反应机制来生存,这对于理解寄生虫生物学尤其重要。”
该研究为开发更好的工具来研究 RNA 修饰及其在耐药性中的作用奠定了基础,同时为药物开发开辟了新途径。 RNA修饰酶,尤其是那些与耐药性相关的酶,目前尚未得到充分研究,它们是开发新的、更有效的药物和疗法的有吸引力的靶点。
通过阻碍寄生虫操纵这些修饰的能力,可以防止耐药性的产生。 SMART AMR 的研究人员正在积极探索和开发对病、细菌、寄生虫和癌症中 RNA 修饰的小分子和生物疗法。
 跳动城乡网
跳动城乡网